复发型多发性硬化症新药!S1P1受体调节剂ponesimod的研发之路

复发型多发性硬化症(remitting multiple sclerosis,RMS)是一种中枢神经系统的慢性炎性自身免疫性疾病,临床主要表现为疲倦、视力衰退、行走不稳、身体麻木、眩晕甚至小便失禁等,可严重影响患者日常生活,且女性发病率至少是男性的2倍。在发病15年后,患者大多需要辅具等装置,30%需以轮椅代步[1]。对大多数患者来说,RMS发病早期会有多次复发和缓解,且随着时间的推移,可能出现缓解不完全导致的渐进性恶化[2]。临床上治疗RMS的口服药物有芬戈莫德、特立氟胺、富马酸二甲酯 [3]。
Ponesimod是特异性鞘氨醇-1-磷酸1(sphingosine-1-phosphate 1,S1P1)受体调节剂,是临床治疗RMS新药,适用于治疗成人RMS,包括临床孤立综合征、复发-缓解性疾病和继发性进行性疾病[4-6]。
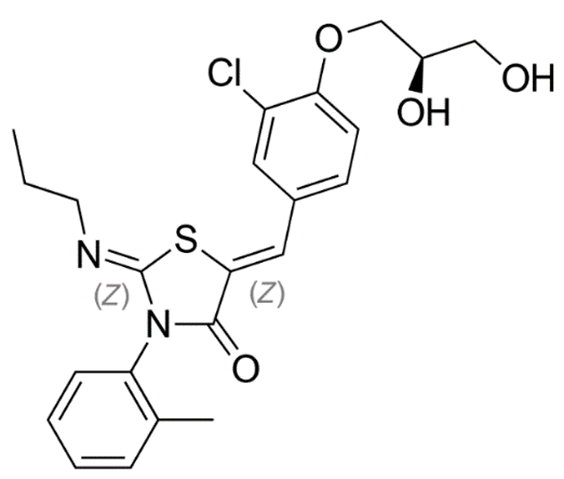
图1 Ponesimod分子结构式
Ponvory:第一个获FDA批准的DMT

图2 FDA批准ponesimod片剂上市官网截图
2021年3月18日,美国食品药品监督管理局(FDA)批准ponesimod片剂上市,其商品名为Ponvory®。
2021年5月24日,欧盟委员会(EC)批准在所有27个成员国和3个欧洲经济区国家(挪威、冰岛和列支敦士登)可临床使用ponesimod治疗成人RMS。
Ponvory成为第一个,也是唯一获得FDA批准的针对现有口服治疗药物的疾病修饰疗法(disease modification therapy,DMT)[7]。
Ponesimod的研发之路
Ponesimod由瑞士Actelion生物制药公司首先研制,并于2016年11月加入美国强生公司创办的治疗自身免疫性疾病协作组,拟开发为新的治疗药物。
2017 年1月,强生公司将Actelion公司的ponesimod及多个在研候选品种纳入强生公司全资子公司,并责成其控股的杨森制药公司全力开发ponesimod。

图3 Ponesimod的Ⅲ期临床试验相关研究成果
基于ponesimod不同的适应症,杨森制药公司开展了多项临床试验。首先,为验证ponesimod治疗MS、牛皮癣和抗移植物抗排异等的效果,共纳入3584例受试者,开展了14批临床试验。其中,Ⅰ期临床试验6批共227例;Ⅱ期临床试验5批共1211例;Ⅲ期临床试验3批共2146例[4]。其中,验证治疗MS的临床试验,有11批次,纳入3191例受试者,其中,Ⅰ期临床6批227例;Ⅱ期临床2批 818例;Ⅲ期临床试验3批 2146例[5]。在美国FDA 批准ponesimod片上市之际,所有临床试验接近全部完成,少数批次试验正处于数据处理阶段,开发公司也在JAMA Neurology上公开发表了Ⅲ期临床试验结果,该期刊影响因子为18.302[6]。
2019年9月,杨森公司在欧洲多发性硬化症(multiple sclerosis,MS)治疗与研究委员会第35届会议上公布了ponesimod的Ⅲ期临床试验研究结果。该研究在RMS成人患者中开展,将ponesimod与法国赛诺菲制药公司治疗多发性硬化症新药特立氟胺进行对比试验。该研究结果表明,ponesimod对患者临床疗效的主要观察指标或次要指标均有显著的改善效果。
2020年3月4日,杨森制药公司向欧洲药品管理局(EMA)提交营销授权应用(marketing authorization application,MAA)申请,申请批准将ponesimod用于治疗成人RMS。
同年3月22日,杨森制药公司向FDA递交新药上市申请(new drug application,NDA)。
2021年3月18日,FDA批准ponesimod片剂上市,商品名为Ponvory,用于治疗成人RMS。
Ponesimod:改善RMS患者年复发率、疲劳症状及磁共振成像结果

一项多中心、随机、双盲、阳性对照的Ⅲ 期临床试验(NCT02425644),比较了ponesimod 20 mg与特立氟胺14 mg在RMS患者中的疗效、安全性和耐受性[8]。该试验有162个中心,随机分布在北美、欧洲、墨西哥、以色列和土耳其等28个国家,纳入研究的RMS患者需满足以下至少1点:①1年内复发至少1次;②2年内至少复发2次;③半年内至少有1个钆增强磁共振成像(magnetic resonance imaging,MRI)显示的T1加权影像病变。患有原发性进行性MS患者除外。该试验共纳入1133例患者,随机分为ponesimod组(n=567)和特立氟胺组(n=566)。该研究显示,ponesimod组年复发率(0.202%)较特立氟胺组(0.290%)相对降低30.5%(P<0.001);与基线相比,ponesimod组治疗第108周新增的钆增强MRI显示的T1、T2病变数量较特立氟胺组分别降低58.5%、55.7%(P<0.0001)。试验结果表明ponesimod在改善患者年复发率、疲劳症状及磁共振成像方面均优于特立氟胺[9]。
展望

罕见病是健康领域的重大挑战之一,给人类社会发展带来沉重负担。尽管罕见病患病率低,但由于我国人口基数大,估测目前仍至少有1680 万人罹患罕见病[9]。国家卫生健康委员会等5部门于2018年5月联合制定了《第一批罕见病目录》并将MS纳入其中,但现阶段MS尚无法完全治愈,其治疗方式仍以缓解期的DMT为主。
与其他已上市的S1P1受体调节剂相比,ponesimod对S1P1受体的选择性更高,可缓解中枢神经系统炎症,降低不良反应发生率。现有临床试验证明ponesimod可有效改善多发性硬化症患者的疾病状态,但其长期用药的安全性及耐受性还有待进一步研究,相信在完善相关数据后,ponesimod有望成为治疗成人RMS的首选S1P1受体调节剂[10]。
参考文献
[1] TULLMAN MJ. Overview of the epidemiology,diagnosis,and disease progression associated with multiple sclerosis[J]. Am J Manag Care,2013,19(2 Suppl):S15-S20.
[2] 张秀颖,白秋江,李岩峰,等. 治疗复发性多发性硬化症新药:特立氟胺[J]. 中国药师,2013,16(12):1928-1930.
[3] 程睿,徐飞虎,周胜军,等. 多发性硬化症的药物治疗进展[J]. 中国新药杂志,2014,23(23):2748-2752.
[4] MARKHAM A. Ponesimod:first approval[J]. Drugs, 2021, 81(8): 957-962.
[5] FDA. PonvorytmTM (ponesimod) tablets, for oral use[EB/OL].(2021-03-26)[2022-01-15]. https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/213498s000lbl.pdf.
[6] KAPPOS L, FOX RJ, BURCKLEN M, et al. Ponesimod compared with teriflunomide in patients with relapsing multiple sclerosis in the active-comparator phase 3 OPTIMUM study:a randomized clinical trial[J]. JAMA Neurol, 2021, 78(5): 558-567.
[7] 陈本川. 复发型多发性硬化症疾病修饰治疗新药——庞西莫德(ponesimod)[J]. 医药导报, 2021, 40(10): 1454-1463.
[8] Clinical Trials. NCT02425644[EB/OL]. (2020-05-27)[2021-01-15]. http://clinicaltrials.gov/ct2/show/results/NCT02425644?term=NCT02425644&draw=2&rank=1.
[9] 赵艺皓, 王翔宇, 丁若溪, 等. 罕见病疾病负担研究进展与医疗保障政策的方向抉择[J]. 中国卫生事业管理, 2018, 35(9): 644-648, 656.
[10] 刘杨, 张海英. 治疗复发型多发性硬化症新药——珀奈莫德[J]. 临床药物治疗杂志, 2021, 19(10): 28-32.

药圈网写手 ·
刘莉莹
主管药师
主要从事新药研发,擅长中药提取分离结构鉴定等方向
药圈网写手库
团队介绍:
2020年药圈网组织了“药师·合理用药·健康守护”征文活动,征集到全国各地优秀的写手,组建了一支医师、药师写手队伍。职业涵盖了临床、药学、培训、质量管理等;汇集了中医药产业政策解读者、基层卫生改革观察员、合理用药科普推广强手;致力于科室管理、药学监护、合理用药、药事管理等内容分享。欢迎更多写手加入我们!药圈网,一个属于医药人的圈子

关注公众号:拾黑(shiheibook)了解更多
[广告]赞助链接:
四季很好,只要有你,文娱排行榜:https://www.yaopaiming.com/
让资讯触达的更精准有趣:https://www.0xu.cn/
 关注网络尖刀微信公众号
关注网络尖刀微信公众号随时掌握互联网精彩
- 1 从“水之道”感悟“国之交” 7904756
- 2 台当局被曝和日本出现军事勾连迹象 7809302
- 3 1818名明星网红等人查补税款15.23亿 7712981
- 4 全国冰雪季玩法大盘点 7617407
- 5 女子遭75岁丈夫家暴 村民发声 7519684
- 6 周星驰《鹿鼎记》重映首日票房仅18万 7424313
- 7 净网:网民造谣汽车造成8杀被查处 7331390
- 8 政治局召开会议 分析明年经济工作 7234622
- 9 退学北大考上清华小伙被欠家教费 7135814
- 10 流感自救抓住“黄金48小时” 7039749







 药圈网
药圈网







